Source : http://www.fedecardio.org/rester-en-bonne-sante/les-deux-formes-de-diabete
L’insulinorésistance, c’est quoi ?
On peut la définir comme une incapacité fonctionnelle des cellules corporelles (surtout celles du foie, des muscles striés et des tissus graisseux) à réagir à l’action de l’insuline. Ces cellules cible y deviennent insensibles : on dit qu’elles résistent à l’insuline.
On sait que normalement, l’insuline a pour fonction, en agissant sur les récepteurs insuliniques accrochés aux parois de ces cellules, d’ouvrir leurs portes par une sorte de clé, afin que le glucose circulant puisse être transporté à l’intérieur des cellules (par le système des GLUT, transporteurs de glucose). Ce glucose pénètre ainsi dans le cytoplasme des cellules, d’abord pour y être métabolisé afin d’y fournir de l’énergie, ensuite pour y être stocké sous forme de glycogène ou de graisses.
En cas d’insulinorésistance, le glucose-carburant n’entre plus que partiellement dans les cellules devenues moins sensibles à l’insuline. Sans glucose, ces cellules s’affament. Par contre, le glucose qui n’est plus éliminé de la voie sanguine, s’y accumule et fait monter la glycémie.
Cette poussée d’hyperglycémie, nous le savons, stimule les cellules β du pancréas à produire davantage d’insuline, ce qui finit par déverrouiller les portes bloquées pendant encore un certain temps. Ainsi, les cellules sont réapprovisionnées en glucose malgré tout et la glycémie redescend, bien que plus lentement, à un niveau normal. Un certain équilibre s’installe pour un temps encore. A ce stade, on parle d’intolérance au glucose, mais pas encore de diabète.
Ce n’est que plus tard, à force de matraquage des cellules β en les forçant à produire toujours plus d’insuline, que celles-ci s’épuisent progressivement, de sorte que toutes les cellules du corps nécessitant du glucose finissent par garder leurs portes d’entrée fermées au glucose, puisque la quantité toujours plus grande d’insuline requise pour les ouvrir, n’est plus disponible. Ainsi, la glycémie reste haute en permanence et le diabète de type 2 s’installe.
L'insulinorésistance se fait à 2 niveaux [1]:
-
Au niveau hépatique : l’insensibilité des cellules du foie à l’insuline se traduit par :
-
Une suppression insuffisante de la production de glucose par le foie (suppression insuffisante de la néoglucogenèse) : le foie va donc augmenter sa production de glucose ;
-
Une captation insuffisante du glucose par le foie.
-
Au niveau périphérique : une captation insuffisante du glucose par les tissus périphériques, comme par exemple :
-
Les muscles striés (muscles squelettiques, muscle cardiaque);
-
Les tissus adipeux (cellules graisseuses ou adipocytes).
A tous les niveaux, l’insulinorésistance fait donc monter la glycémie.
Les causes et facteurs d’aggravation de l’insulinorésistance[2].
En réalité, les causes intimes de l’insulinorésistance ne sont pas encore entièrement élucidées. Son origine est plurifactorielle. Certains facteurs d’aggravation sont aussi de vraies causes, mais d’autres ne sont que des épiphénomènes.
Pour Bernstein[3], il existe au moins cinq causes à l’insulinorésistance :
-
L’hérédité ;
-
Une glycémie trop élevée ;
-
L’obésité (Indice de Masse Corporelle >25), surtout la surcharge pondérale androïde ;
-
L’inflammation et l’infection ;
-
La déshydratation.
Nous y ajouterons :
-
L’hyperinsulinémie
-
L'augmentation du taux d'acides gras libres et l’hypertriglycéridémie.
L’hérédité :
Ce qui est à peu près certain est l’implication à un degré variable de l’expression génétique. Le fait qu’il y ait un terrain familial est une notion établie depuis longtemps. La race peut jouer un rôle également : les Noirs, les Amérindiens, les Hispaniques, les Asiatiques peuvent y être plus sensibles[4]. Mais l’hérédité n’explique pas tout. Elle n’est qu’un des nombreux facteurs responsables de la perte de sensibilité à l’insuline [5].
Les autres mécanismes responsables se situent à différents niveaux du métabolisme insulinique, dont une altération des récepteurs à insuline des cellules cible décrites plus haut. Physiologiquement, ces récepteurs sont extrêmement sensibles aux taux circulant d’insuline, mais également à ceux du glucose, des lipides, etc.
L’hyperinsulinémie :
On a constaté qu’une insulinémie trop élevée (plus de 20 μU d’insuline/ml) peut diminuer fortement le nombre de récepteurs insuliniques : si la stimulation insulinique est continue et intense, on a calculé que 10% des récepteurs insuliniques sont perdus à chaque cycle du récepteur[6]. Leur nombre total en est réduit de façon importante. Un autre mécanisme possible est l’activité réduite de ces récepteurs par une altération de leurs molécules[7]. Cette régulation négative liée à l’hyperinsulinémie explique pour une part l’installation de l’insulinorésistance[8].
Par ailleurs, l'hyperinsulinémie de base freine la production hépatique de glucose (néoglucogenèse).
En cas d'hypoinsulinémie postprandiale, la sécrétion d'insuline est insuffisante pour assurer la captation ainsi que le stockage musculaire et hépatique du glucose.
Ces deux derniers facteurs (hyperinsulinémie de base et l’hypoinsulinémie postprandiale) aggravent l'insulinorésistance, la première en diminuant le nombre de récepteurs et la seconde en abaissant la capacité du transport de glucose.
L’hyperglycémie entraîne et aggrave l’insulinorésistance:
De nombreux travaux cliniques et expérimentaux ont montré que l'hyperglycémie chronique altère progressivement l'insulino-sécrétion et diminue l'action périphérique de l'insuline, ce qui conduit à l'auto-aggravation du diabète non-insulino-dépendant.
Une situation hyperglycémique augmente l’insulinorésistance musculaire et adipeuse. Cet effet est dû à une diminution de la translocation des transporteurs du glucose GLUT4 et GLUT1 entre les microsomes de faible densité du compartiment intracellulaire et la membrane.
Donc plus la glycémie s’élève, plus il y a insulinorésistance et plus le diabète s’aggrave. Ainsi s’instaure un parfait cercle vicieux qui est attribué à des défauts post-récepteurs dans l'utilisation du glucose[9].
Par conséquent, les diabétiques T2, comme les T1 d’ailleurs, ont un double intérêt à garder leur glycémie la plus basse possible :
La surcharge pondérale importante :
Une obésité androïde liée à une hyperleptinémie [10], [11], [12], chez les sujets susceptibles de développer un diabète de type 2, entraîne une insulinorésistance, avec hyperinsulinisme.
Non seulement l’obésité est une de causes probables, elle est certainement un facteur aggravant très important de l’insulinorésistance.
Pour un indice de masse corporelle (IMC) à la limite supérieure de la normale (23 à 24,9), le risque relatif est déjà plus que doublé (2,67). Avec un surpoids important (IMC entre 30 et 34,9), le risque relatif passe à 20,1 et avec un surpoids sévère (IMC supérieur à 35) à 38,8.
Plus important encore que l’IMC, la répartition des graisses sous la peau de l’abdomen et autour des viscères (et qui est appréciée par le tour de taille) augmente le risque de développer un DNID (diabète non insulinodépendant) dès que le tour de taille dépasse 80 cm chez la femme et 94 cm chez l’homme [13].
La rapide augmentation de l’obésité chez les enfants et les adolescents au cours des trois dernières décennies du XXe siècle a été suivie par l’apparition de cas de DNID à un âge de plus en plus précoce, caractérisé par une aggravation de l’insulinorésistance dès la puberté, et plus encore chez les filles que chez les garçons[14].
L'augmentation du taux d'acides gras libres :
Majorée par la surcharge pondérale androïde, c’est surtout l’augmentation des graisses saturées qui aggrave l'insulinorésistance.
Selon une récente étude américaine[15], ce sont les glucides qui font monter le niveau de graisses saturées dans le sang, pas les graisses alimentaires. Doubler, voire même presque tripler la quantité d’acides gras saturés dans l’alimentation ne contribue pas à faire grimper le niveau sanguin d’acides gras saturés. En revanche, une augmentation de la quantité de glucides alimentaires entraine l'élévation d’un acide gras dans le sang (l’acide palmitoléique), qui a été lié à un risque accru d’insulinorésistance, de diabète et de maladie cardiaque[16].
Les acides gras polyinsaturés de type oméga 3 par contre, améliorent l’insulinorésistance.
L'hypertriglycéridémie :
C'est l'anomalie la plus souvent rencontrée en cas de syndrome métabolique et chez les diabétiques de type 2. Un taux élevé de triglycérides est non seulement une cause directe d’insulinorésistance[17], il contribue également à la formation de dépôts sous forme de plaques[18] (athéromes) sur les parois des artères de gros ou moyen calibre (athérosclérose). Il est souvent associé à une diminution des HDL (High Density Lipoproteins) ou «bon» cholestérol[19].
Les personnes maigres et en bonne condition physique sont généralement fort sensibles à l’insuline et ont des taux sanguins très bas de triglycérides, mais aussi d’insuline. Cependant, leur niveau de triglycérides augmente après un repas riche en glucides, car l’excès de glucose est converti en graisses. Plus la quantité de (mauvaise) graisse abdominale est élevée par rapport à la masse maigre (muscles), moins la personne deviendra sensible à l’insuline. En cas d’obésité, des taux élevés de triglycérides sont présents en permanence.
On a constaté expérimentalement que l’injection de triglycérides ou d’acides gras saturés dans la veine porte (qui irrigue le foie) chez des athlètes très sensibles à l’insuline, provoque chez ceux-ci temporairement de l’insulinorésistance. A noter toutefois que l’insulinorésistance, tout comme les autres facteurs à risque donnant lieu aux complications du diabète, peut être inversée en mangeant très peu de glucides, en normalisant la glycémie et en maigrissant[20].
L’inflammation et l’infection :
Une infection grave dérègle le diabète. De plus, le diabète rend plus sensible aux infections. Voici encore un cercle vicieux des plus néfastes qui s’annonce.
Tous les cliniciens qui s’occupent de diabète savent que celui-ci s’aggrave en cas d’inflammation, d’infection ou de certaines maladies. Notamment, chez les patients insulinodépendants, tant ceux de type 1 que de type 2, les besoins en insuline peuvent monter considérablement dans ces cas-là.
Si l’insulinorésistance peut être renforcée par l’obésité et l’augmentation de certains lipides, c’est probablement par la production du facteur de nécrose tumorale α, TNFα (de l’anglais tumor necrosis factor α), une importante (adipo)cytokine impliquée dans l'inflammation. L’inflammation est le résultat d’une réponse de notre système immunitaire à une agression, telle une infection virale ou bactérienne. Indépendamment de la graisse abdominale, d’autres causes d’inflammation pouvant générer l’insulinorésistance sont les maladies infectieuses, les maladies auto-immunitaires telles que le lupus érythémateux systémique, l’arthrite rhumatoïde juvénile, la maladie cœliaque (l’intolérance au gluten). Le résultat net de l'ensemble de ces perturbations par les cytokines pro-inflammatoires est encore une fois le début d'un cercle vicieux : plus d'adipocytokines conduit à plus d'insulinorésistance et donc à une hausse (surtout) du tissu graisseux viscéral, qui à son tour génère une synthèse plus grande encore de cytokines, etc…[21].
Expérimentalement, une aggravation brusque de l’insulinorésistance peut aussi être provoquée par l’injection d’interféron γ (IFNγ), une autre protéine (glycoprotéine) de la famille des cytokines. L’IFNγ, joue un rôle immunitaire crucial contre les infections virales et certaines infections bactériennes et protozoaires[22].
Pour déceler une inflammation, certains marqueurs de l’inflammation peuvent s’avérer positifs lorsqu’ils sont testés dans le sang, mais ce n’est pas toujours le cas, loin s’en faut. Il s’agit essentiellement de : la vitesse de sédimentation, la CRP (C-reactive protein) et surtout la hsCRP (ou CRP hautement sensitive), la β2-microglobuline, la ferritine, le complément C3, le TNFα, le fibrinogène sérique. En cas de positivité d’un ou de plusieurs de ces tests, un examen plus approfondi par un infectiologue ou un immunologue s’impose.
La déshydratation aggrave l’insulinorésistance
Une déshydratation rapide ne doit jamais être prise à la légère, surtout chez les enfants, les personnes âgées et encore plus s’ils sont diabétiques. C’est une urgence absolue. Une déshydratation aigue risque de favoriser la survenue d’un coma diabétique par un mécanisme où hyperglycémie et insulino-résistance sont étroitement imbriquées.
Quelle que soit la cause de la déshydratation : des vomissements continuels, une diarrhée profuse, une transpiration abondante lors d’une forte fièvre ou d’une canicule chez un bébé ou une personne âgée insuffisamment réhydratée, toutes ces situations seront vraisemblablement accompagnées d’une montée de la glycémie.
Pourquoi ? Déjà à cause de l’infection si celle-ci est la cause de la déshydratation. D’autre part, lorsque qu’un compartiment du corps se vide de ses liquides, l’équilibre fonctionnel (l’homéostasie) fera que le liquide perdu soit remplacé par du liquide venant d’ailleurs et où il se trouve en abondance, par exemple le sang et la circulation sanguine qui irrigue tous les organes et tissus. Le sang perdra ainsi une partie de son fluide par diffusion vers les parties qui en manquent. Le sang, beaucoup plus concentré, garde néanmoins le glucose : la glycémie monte. Et l’insulinorésistance en même temps.
Mais ce n’est pas tout. Si le volume sanguin diminue (hypovolémie) à cause d’une perte conséquente de liquides, toutes les petites artères et artérioles, qui se trouvent en périphérie des organes et tissus, ne sont plus aussi bien irriguées. Cela a pour conséquence que ni le glucose, ni l’insuline n’atteignent suffisamment les cellules irriguées par ces petits vaisseaux. C’est alors comme si tous ces tissus moins bien fournis deviennent parfaitement insulinorésistants, puisque le glucose ne pénètre plus leurs cellules. Ainsi, la glycémie continue de s’élever.
Plus on devient résistant à l’insuline, plus la glycémie s’élève, et vice-versa. Un nouveau cercle vicieux particulièrement dangereux s’instaure…
En effet, ce n’est toujours pas tout : quand le taux sanguin du glucose est élevé, on urine. Et en urinant, on se déshydrate encore plus, on devient encore plus insulinorésistant, et, bien-sûr, la glycémie monte encore, pour finalement atteindre des sommets vertigineux.
Que se passe-t-il alors : soit ces cellules périphériques meurent par manque de glucose-carburant (ou d’oxygène), soit elles se mettent à brûler leur graisse. Dans ce dernier cas, des corps cétoniques sont fabriqués par le métabolisme des graisses. Ceci fait uriner encore plus le patient pour qu’il se débarrasse des corps cétoniques, et il atteint un nouveau degré de déshydratation. C’est ainsi qu’on approche finalement le coma acido-cétosique ou une insuffisance rénale aigue nécessitant une dialyse[23].
La déshydratation, on le voit, peut devenir dramatique très rapidement : n’hésitez pas d’appeler votre médecin ou les urgences à temps !
*
* *
Les autres facteurs à risque de l’insulinorésistance
A côté des vraies causes, il existe de nombreux autres facteurs à risque pouvant augmenter ou aggraver l’insulinorésistance. En voici les principaux :
Une mauvaise alimentation menant à l’obésité[24]
- Un apport calorique trop important menant à une surcharge pondérale même légère est préjudiciable. Dans ce cas, il est donc nécessaire de maigrir à raison de 1 à 2 kg par mois à peu près, jusqu’à l’obtention d’un poids normal[25].
- Pour ce qui est des glucides, nous préconisons de les réduire à maximum 45 % de l’apport énergétique total et d’abandonner les 50 à 60 % encore préconisés aujourd’hui par les instances officielles, car cela s’avère néfaste pour l’équilibre métabolique en engendrant une insulinorésistance par élévation des triglycérides.
- Nous recommandons également de favoriser les glucides à index et charge glycémique réduits ou modérés[26]. En effet, les sucres et amidons à index glycémique élevé augmentent fortement l’insulinorésistance.
- Notons également qu’une alimentation riche en fructose, présent dans les fruits mais aussi dans miel et le sucre de table (saccharose), diminue la stimulation de l’insuline et le transport du glucose. Pris en trop grande quantité, le fructose est néfaste en augmentant les triglycérides et induit une insulinorésistance. Il fait grossir, et endommage le foie[27]. Afin d’éviter cet inconvénient, la quantité de fructose ne devrait pas dépasser 10 à 15 % de la ration calorique journalière. Nous préconisons de le prendre sous forme de fruits entiers en quantité modérée (un fruit ne contient en moyenne que 10 gr de fructose) et de l’éviter le plus possible sous sa forme pure en poudre cristallisée ou en sirop (ce sont souvent les sucres ajoutés de la nourriture industrielle).
- La bonne alimentation en graisses (lipides) et en protéines a fait l’objet de plusieurs articles déjà parus[28], [29]. Rappelons la clé de répartition proposée :
Lipides : 40% de l’apport calorique total, dont :
10% pour les graisses saturées
10% pour les graisses polyinsaturées (surtout les ω3)
20% pour les graisses monoinsaturées (p.ex. l’huile d’olive)
Protéines : 15% de l’apport calorique total (1 g/kg/jour).
Le style de vie sédentaire ou manque d’exercice physique.
Les mécanismes de la protection vis-à-vis du diabète de type 2 par l’activité physique sont à la fois directs, par le biais de l’amélioration de la sensibilité à l’insuline, et indirects par le contrôle du poids et le maintien de la composition corporelle. L’entraînement physique est associé à une augmentation de la sensibilité à l’insuline même en l’absence de modification pondérale. La perte de poids peut amplifier cet effet. L’amélioration de la sensibilité à l’insuline par l’entraînement est observée même dans le cas de la pratique d’activités physiques d’intensité modérée, mais apparaît de courte durée (quelques jours au plus). Le caractère régulier de l’activité est donc absolument essentiel d’où l’importance des aspects concernant la compliance aux recommandations[30].
L’âge :
Le risque augmente passé l'âge de 40 à 45 ans. Cela correspond plus ou moins à l’âge où apparaît généralement le diabète de type 2, associé à l’insulinodépendance.
Un poids élevé à la naissance ou macrosomie (> 4 kg).
La mère a généralement présenté un diabète gestationnel qui peut disparaître après la grossesse. Cependant, elle reste candidate au diabète de type 2 (un cas sur trois). Chez les bébés filles surtout, le risque métabolique survient également plus tard, pas chez les garçons[31].
L’usage de corticostéroïdes et de certains autres médicaments
Par exemple: la glucosamine, la rifampicine, l’isoniazide, l’olanzapine, la rispéridone, les progestagènes, la méthadone, plusieurs antirétroviraux, les statines[32], [33]).
Les corticoïdes induisent une insulinorésistance. Ils réduisent l’action de l’insuline en accroissant la néoglucogenèse et en diminuant les possibilités de captation et d’utilisation du glucose par les tissus périphériques (muscle surtout). De plus, ils inhibent la sécrétion de l’insuline. Les études cliniques, parfois discordantes, tendent à montrer que la probabilité d’observer des glycémies élevées chez un diabétique traité par corticoïdes est plus faible si le diabète est bien équilibré, avec un taux d’HbA1c inférieur à 6,5 % (48 mmol/mol). À l’inverse, le déséquilibre observé est plus important si le taux d’HbA1c dépasse 8 % (64 mmol/mol), et lorsque l’âge et l’indice de masse corporelle sont élevés[34].
Le tabagisme.
Non seulement le tabagisme est un facteur de risque cardio-vasculaire majeur, il est associé à des anomalies de la fonction endothéliale et du métabolisme lipidique semblables à celles retrouvées dans le syndrome métabolique lié à l’insulinorésistance. Des études ont cherché à démontrer un lien entre tabagisme et insulinorésistance, puis entre tabagisme et diabète de type 2. Bien que leurs résultats ne soient pas tous concordants, le fait de fumer semble effectivement être associé à une diminution de la sensibilité à l’insuline, proportionnelle à l’intensité de la consommation de cigarettes[35].
L’absorption aiguë d’alcool.
Il existe des relations entre consommation d'alcool, insulinorésistance, incidence du diabète de type 2 et incidence des maladies cardiovasculaires chez le diabétique de type 2. En effet, si plusieurs travaux montrent que l'absorption aiguë d'alcool induit plutôt une insulinorésistance, de nombreuses études épidémiologiques suggèrent, au contraire, qu'une exposition chronique à dose modérée est associée à une amélioration de l'insulinosensibilité. En outre, un certain nombre d'études prospectives montrent un rôle protecteur d’une prise régulière mais modérée d’alcool vis à vis du développement du diabète et de la coronaropathie du diabétique de type 2. Il s’agit d’un véritable paradoxe[36].
Le stress.
L'activation du système adrénergique et l'augmentation de la sécrétion de cortisol ont été de longue date démontrées au cours de situation d'agression ou de situation stressante aiguë surtout.
Les glucocorticoïdes influencent la régulation pondérale. Ils réduisent la captation de glucose par le muscle et favorisent donc l'insulinorésistance musculaire. Des études récentes montrent que les glucocorticoïdes ont également un impact sur les neuromédiateurs de la prise alimentaire[37].
Maladies associées à l’insulinorésistance
Le syndrome de surcharge (poly)métabolique, syndrome X ou prédiabète.
L’insulinorésistance s’insère entièrement dans le cadre du syndrome de surcharge métabolique. Ce dernier est caractérisé par la présence d'au moins trois des anomalies suivantes[38]:
-
Une obésité avec BMI[39] - IMC[40] > 30 kg/m²
-
obésité abdominale (androïde) : tour de taille ≥ 94 cm chez l'homme, ≥ 80 cm chez la femme c.à d. généralement avec un rapport du tour de taille sur le tour de hanches supérieur à 0,85 pour une femme et de 0,9 pour un homme
-
hypertriglycéridémie >145 mg/dL ou >1,45 g/L
-
taux bas de HDL-cholestérol (<35 mg/dL chez l'homme et < 40 mg/dL chez la femme)
-
une HTA[41] (elle-même définie par l'existence d'un traitement ou une PAS[42] >140 mm Hg ou une PAD[43] >90 mm Hg)
-
une intolérance au glucose; glycémie à jeun >110 mg/dL ou >6,1 mmol/L
-
une microalbuminurie
-
La mesure du cholestérol est un mauvais critère car 50 % des patients présentant une maladie cardiovasculaire ont un cholestérol normal[44].
Rappelons que dans le syndrome métabolique ou prédiabète, les sujets atteints ont encore une glycémie normale car bien que l'insulino-résistance doive normalement entraîner une hyperglycémie, une sécrétion accrue d'insuline maintient l’euglycémie.
Ceci conduit donc à une situation hyperinsulinémique transitoire (un sujet est hyperinsulinique si son sang contient plus de 20 μU d’insuline/ml) qui exacerbe les effets délétères de cette hormone sur l’ensemble de l’organisme. En particulier, elle est à l’origine de dyslipidémie, d’une hyper-agrégation plaquettaire et d’une inhibition de la fibrinolyse qui conduit au développement de conditions pro-thrombiques, faisant le lit des complications vasculaires accompagnant l’état diabétique. L’insuline en excès perturbe également la thermogenèse (déficiente chez le diabétique) et est à l’origine d’une formation de radicaux libres oxygénés très réactifs impliqués dans la dégradation des protéines, entre autres celles de la membrane basale. L’insulino-résistance se trouve donc ici associée à l’hyperinsulinisme, aux maladies coronariennes et à l’hypertension artérielle[45].
Comme le diabète de type 2, le syndrome métabolique est en partie d'origine génétique (pour un tiers environ) et en partie environnementale. La part héréditaire dans cette affection semble surtout concerner la résistance à l'insuline. L'idéal serait de pouvoir poser le diagnostic dès ce stade prédiabétique pour améliorer le traitement de cette pathologie et son évolution à long terme[46].
Le diabète de type 2 non-insulinodépendant (DNID)
Le diabète de type 2 n’est rien d’autre qu’une suite logique du syndrome métabolique[47]. Dans ce sens, il apparait que l'apparition d'un DNID soit, dans l'immense majorité des cas, liée non pas à une carence en insuline mais au contraire à une hyperinsulinémie déclenchée par un insulino-résistance périphérique (refus musculaire du glucose). Le diagnostic du DNID se fait 10 ans trop tard[48] !
Pendant longtemps la glycémie reste normale au prix de cet hyperinsulinisme, mais les dégâts rétiniens, coronariens ont déjà commencé.
Le tissu adipeux abdominal et viscéral étant très sensible à la lipogenèse induite par l'insuline, on retrouve cette obésité androïde, marqueur maintenant reconnu du risque cardio-vasculaire[49].
Le diabète insulino-dépendant (DID) de type 1 ou de type 2
L’insulinorésistance est un phénomène clairement lié au syndrome métabolique et au diabète de type 2 (DNID). En cas d’insulinodépendance (DID), il n’y a plus de production suffisante d’insuline, soit par épuisement des cellules β en phase finale du diabète de type 2, soit par destruction de celles-ci dès le début du diabète de type 1. Les causes et les mécanismes physiopathologiques des deux types de diabète n’étant pas les mêmes, nous ne retrouverons donc pas les mêmes causes d’insulinorésistance.
Par exemple, les diabétiques de type 1 comptent beaucoup moins d’obèses que ceux du type 2 et par leur absence presque totale d’insuline, l’excès de glucose dans la voie sanguine ne sera, ni récupéré par les cellules réceptrices, ni converti en graisse. Le très important facteur d’insulinorésistance que constitue la surcharge pondérale n’est donc pas à l’ordre du jour en cas de diabète de type 1. Par contre, une forte hyperglycémie, une inflammation, une infection grave, une déshydratation, un stress intense peuvent tout aussi bien nécessiter des doses d’insuline nettement plus élevées dans le type 1.
D’autre part, l’insuline injectée en cas de DID est une protéine non naturelle. Celle-ci peut se faire détruire en partie par notre système immunitaire qui se défend contre cet élément étranger. Dans ce cas la demande d’insuline augmentera également.
Ces deux cas évoquent une forme d’insulinorésistance élargie à d’autres causes que celle, classique, d’un défaut postrécepteur d’utilisation du glucose.
Le diabète gestationnel
Le diabète gestationnel est un état d'intolérance au glucose, quelle que soit sa sévérité, apparu au cours de la grossesse chez une femme sans diabète sucré connu antérieurement. Il peut néanmoins être révélateur d'un diabète antérieur. Le diabète gestationnel peut exposer à des complications maternelles et fœtales potentiellement sévères. Il apparaît classiquement entre la 24e et la 28e semaine d'aménorrhée (absence de règles), correspondant à la sécrétion de l'hormone lactogène placentaire (HPL, Human placental lactogen en Anglais) par le placenta, responsable d'insulinorésistance chez la mère[50].
Les maladies cardiovasculaires : athérosclérose, hypertension artérielle, maladie coronarienne, infarctus du myocarde
Les maladies cardiovasculaires et l’insulinorésistance ayant plusieurs causes en commun à la base (les facteurs alimentaires, des phénomènes inflammatoires, l’obésité, le diabète, la sédentarité, l’hérédité, le stress, le tabac,…), il n’est pas étonnant que ces maladies soient souvent associées.
Certaines maladies du foie
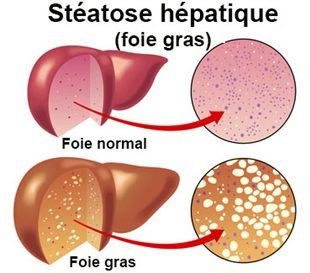
Le surpoids, l’insulinorésistance, le syndrome métabolique et le stress oxydatif, favorisé par la surcharge en fer, sont en cause dans les stéatohépatites[51], tant alcooliques que non alcooliques et toutes les maladies du foie qui en découlent, p.ex. la cirrhose[52]. L'insulinorésistance est aussi fréquente dans l'hépatite C, une infection virale du foie[53].
La surcharge en fer dans les cellules hépatiques pourrait également être responsable d’une insulinorésistance. C’est le cas dans l’hémochromatose, souvent accompagnée de diabète[54].
Le syndrome policystique ovarien, en anglais : polycystic ovary syndrome (PCOS).
L’insulinorésistance hépatique et musculaire est en effet associée au syndrome policystique ovarien, où elle se trouve renforcée par l’obésité et provoque une hyperinsulinémie compensatrice.
Rappelons que le syndrome des ovaires polykystiques est un trouble hormonal fréquent chez les jeunes femmes : 5 à 10 % sont concernées. Ce syndrome est un problème de kystes bénins qui se forment au niveau des ovaires. Ceux-ci peuvent avoir des conséquences diverses :
-
Une hyperandrogénie : une sécrétion trop élevée d'hormones mâles entraîne des signes et symptômes de type masculin ;
-
Une anovulation : l'ovulation ne se fait plus, ou de manière très rare ;
-
Une aménorrhée : l'absence de règles est très fréquente dans ce trouble, elle est la conséquence directe de l'absence d'ovulation ;
-
Une insulinorésistance : souvent le problème ovarien a un retentissement sur le métabolisme en général, et notamment sur la sécrétion d'insuline, qui peut être liée à du diabète et une obésité[55].
Le syndrome de Cushing.
Associé à un hypercorticisme chronique (excès de cortisol) de causes différentes (notamment l’utilisation de stéroïdes), le syndrome de Cushing se manifeste notamment par une obésité chronique de la partie supérieure du corps et sa pathologie comprend entre autres un déséquilibre dans la répartition des graisses, une néoglucogenèse accrue et l’apparition de diabète associé à de l’insulinorésistance[56].
La gastroparésie ou estomac paresseux.
Comme complication chronique du diabète (généralement de type 1, plus rarement de type 2), la gastroparésie est une atteinte de la régulation neuro-végétative de l’estomac liée à l’exposition à une hyperglycémie chronique prolongée (en moyenne 10 ans). Elle est caractérisée par une vidange souvent aléatoirement ralentie du passage du bol alimentaire à travers l’estomac.
Chez les insulinodépendants, l'apport glucidique du repas n'arrive donc plus en phase avec l'injection d'insuline. Chez certains patients, le caractère aléatoire de la synchronisation entre l’action de l’insuline et l’absorption des glucides alimentaires se traduit par la survenue d’hypoglycémies sévères difficiles à maîtriser autant qu’à prévenir.
La gastroparésie peut aussi s’exprimer exclusivement par une instabilité glycémique avec des évènements d’hypoglycémies et d’hyperglycémies aiguës non expliquées[57], aggravant le diabète. Les besoins en insuline peuvent donc varier considérablement et de manière non prévisible.
Quelle est l’approche thérapeutique de l’insulinorésistance ?
Les traitements seront différents selon la cause de l’insulinorésistance. S’il s’agit d’un syndrome (poly)métabolique, celui-ci doit être dépisté et traité le plus tôt possible, du fait du risque élevé de l’évolution vers un diabète de type 2 et de ses complications.
Peut-on inverser l’insulinorésistance ?
Le syndrome polymétabolique d’insulinorésistance est parfaitement réversible, surtout s’il est traité avant l’installation définitive du diabète de type 2. A cet effet, on associe les mesures diététiques visant à obtenir une perte pondérale, un exercice physique régulier et, si nécessaire, certaines médications[58].
Mesures nutritionnelles et perte de poids
Toute perte de poids, même modeste, se fait prioritairement aux dépens du tissu adipeux périviscéral, plus sensible à la lipolyse que les autres sites. Ainsi, un amaigrissement de quelques kilos suffit à améliorer considérablement la sensibilité à l’insuline et les facteurs de risque vasculaire et thrombogène.
En pratique, il convient d’éliminer le plus possible les sucres à absorption rapides à index et charge glycémiques hauts (pain, féculents, pommes de terre, pâtes, riz), de privilégier les glucides à absorption lente (légumes secs, légumineuses, légumes verts, fruits non sucrés...), de ne prendre que les bonnes matières grasses (huile d’olive, huile de colza, oléagineux et poissons gras riches en oméga 3) en éliminant les mauvaises (contenues dans les viandes grasses, charcuteries, acides gras trans, margarines, crèmes, frites-chips, pizzas, feuilletés, viennoiseries, gâteaux...), de prendre suffisamment de fibres alimentaires, tout en limitant la consommation d’alcool (1 à 2 verres de vin rouge par jour au cours des repas).
L’exercice physique régulier
La pérennité d'une masse musculaire active s'obtient en augmentant le débit sanguin musculaire et en maintenant les fibres musculaires suffisamment sensibles à l’insuline. Ceci facilite l’obtention de la stabilité pondérale obtenue par la diététique. Le glucose est mieux transporté et les acides gras libres plus aisément consommés au niveau des fibres musculaires pendant et après l’effort.
Le syndrome (poly)métabolique et ses conséquences sont ainsi bien améliorés par un exercice pratiqué durant 30 minutes 3 à 5 fois par semaine en fonction des possibilités de chacun.
Traitements médicamenteux
En France, aucune médication n’a l’Autorisation de Mise sur le Marché (AMM) dans le syndrome (poly)métabolique. Cependant, la metformine (Glucophage®), dans des essais cliniques randomisés contre placebo, a induit une diminution de l’insulinémie et de la glycémie[59].
Les autres médicaments concernent le traitement du diabète de type 2 et seront discutés plus tard.
A suivre,
Luc Vangermeersch, le 9 mars 2015.
Bibliographie :
[1] http://www.em-consulte.com/en/article/79688 (consulté en janvier 2015)
[3] Bernstein R., «Dr. Bernstein’s Diabetes Solution», Newly Revised and Updated; Ed. Little, Brown and Company, 2011, p.100.
[6] Cycle du récepteur: chaque fois que le complexe insuline-récepteur pénètre dans la cellule par endocytose et, dans les vésicules ainsi formées, l’insuline est dégradée ainsi qu’environ 10% des récepteurs (les 90% restant rejoignant la membrane plasmatique).
[11] http://fr.wikipedia.org/wiki/Leptine (consulté en janvier 2015). La leptine (du grec leptos, mince) parfois dite « hormone de la satiété » est une hormone peptidique qui régule les réserves de graisses dans l'organisme et l'appétit en contrôlant la sensation de satiété. C'est une molécule produite et sécrétée dans la circulation sanguine par les cellules adipeuses (adipocytes). Son action essentielle est de diminuer la prise alimentaire.
[13] Ibidem 6 (consulté en janvier 2015)
[15] Study: Doubling Saturated Fat in the Diet Does Not Increase Saturated Fat in Blood. Ohio State University, Emily Caldwell.
[16] Volk BM, Kunces LJ, Freidenreich DJ, Kupchak BR, Saenz C, Artistizabal JC, Fernandez ML, Bruno RS, Maresh CM, Kraemer WJ, Phinney SD, Volek JS. Effects of step-wise increases in dietary carbohydrate on circulating saturated Fatty acids and palmitoleic Acid in adults with metabolic syndrome. PLoS One. 2014 Nov 21;9(11):e113605. doi: 10.1371/journal.pone.0113605. eCollection 2014.
[18] Les plaques athéromateuses se forment par accumulation segmentaire de lipides, glucides complexes, sang et produits sanguins, tissus adipeux, dépôts calcaires et autres minéraux.
http://fr.wikipedia.org/wiki/Ath%C3%A9rome (consulté en janvier 2015)
[19] La distinction entre « bon » et « mauvais » cholestérol est un sujet controversé.
[32] Cederberg H, Stančáková A, Yaluri N et coll. Increased risk of diabetes with statin treatment is associated with impaired insulin sensitivity and insulin secretion: a 6 year follow-up study of the METSIM cohort. Diabetologia DOI 10.1007/s00125-015-3528-5.
[33] Sattar N, Preiss D, Murray HM et al (2010) Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials. Lancet 375:735–742.
[39] BMI : Body Mass Index
[40] IMC : Indice de Masse Corporelle
[41] HTA : Hypertension artérielle
[42] PAS : Pression artérielle systolique
[43] PAD : Pression artérielle diastolique
[51] Stéatohépatite : inflammation du foie accompagnée de dégénérescence graisseuse (foie gras)
















































/image%2F0673295%2F201307%2Fob_46ba1e_bdbcff82fa665af64995d563d19afded-normal.jpeg)